肿瘤微环境(TME)标志物的高灵敏度检测,对揭示肿瘤进展状态、实现肿瘤区域定位及指导后续干预具有重要意义。然而,TME具有高度复杂性和动态异质性,现有技术在肿瘤区域定位、微环境特征识别和动态监测等方面仍面临挑战。
近日,中国科学院兰州化学物理研究所天然药物与化学测量研究中心海军研究员团队,发展了一种以氧化石墨烯为二维支撑载体的Fe单原子纳米酶(FeNC SAzymes)。与传统平面Fe-N4构型相比,轴向O配位的引入有效打破了对称配位限制,增强了活性中心的电子调控能力(图1)。此外,密度泛函理论计算解析该关键活性能有效降低多酶反应途径的能量势垒,从而提升NOX、POD和GSHOx等多酶样级联相关过程的反应效率,为后续触发后放大效应提供基础(图2)。FeNC SAzymes结构设计使Fe中心的电荷分布和d轨道电子态密度得到优化,从而提升其对反应中间体的吸附与活化能力以及电子转移效率,为实现TME识别、可视化检测和响应研究提供了新方法。
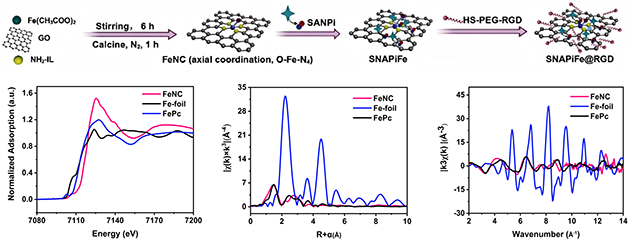
图1.轴向极化FeNC SAzyme的制备与表征
在此基础上,研究团队通过功能分子引入和表面修饰构建了面向TME研究的智能响应纳米平台(SNAPiFe@RGD),利用该平台进一步开展了机制研究。研究发现在细菌定植的4T1荷瘤小鼠模型中,SNAPiFe@RGD在实现肿瘤定位的基础上,还可有效抑制肿瘤内细菌定植,并缓解由其诱导的免疫抑制状态,说明通过对TME变化进行检测和表征,有助于加深对肿瘤进展状态及其微环境演变特征的认识(图3)。同时,SNAPiFe@RGD在完成肿瘤区域及其微环境特征识别的同时,还具备由检测向功能响应延伸的能力。该研究从单原子活性位点调控出发,将TME识别、肿瘤区域可视化定位和后续功能响应有机结合,为其标志物检测和机制研究提供了新思路。
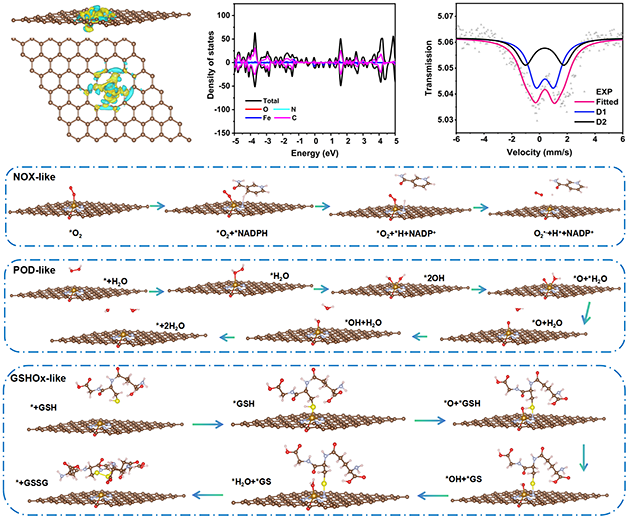
图2.多酶催化原理解析
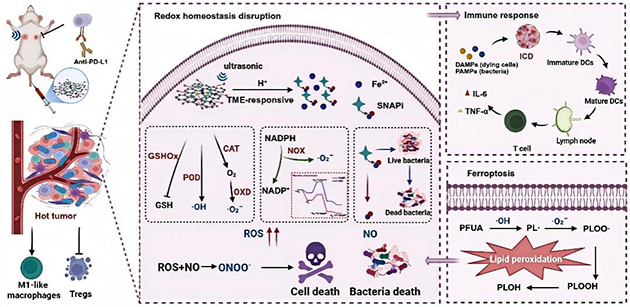
图3.SNAPiFe@RGD SAzymes肿瘤精准定位、同步清除TRIM与肿瘤细胞示意图
相关研究成果以“Axially Polarized O-Fe-N4 Single-Atom Enzyme Drives Clearance of Tumor-Resident Intracellular Microbiota and Potentiates Immunotherapy”为题发表在ACS Nano(2026, 20, 8704-8725)上,兰州化物所景泉博士为论文第一作者,兰州化物所海军研究员、邸多隆研究员和兰州大学汪宝堆教授、新疆大学范仲雄教授为论文共同通讯作者,兰州化物所为第一完成单位。
以上工作得到了国家自然科学基金、中国科学院人才计划项目、甘肃省自然科学基金、甘肃省科技计划和兰州化物所人才项目等支持。